
전기에너지를 휴대용으로 사용하기 위해 개발된 건전지
편해서 아무 생각 없이 사용했는데 아이들과
수업을 하다보면
건전지는 어떻게 만들어지고 언제 만들어지고 등등 질문을 하는 아이들이 있습니다.
그래서 건전지에 대해 알아보려고 합니다.
첫 번째. 건전지의 역사
두 번째.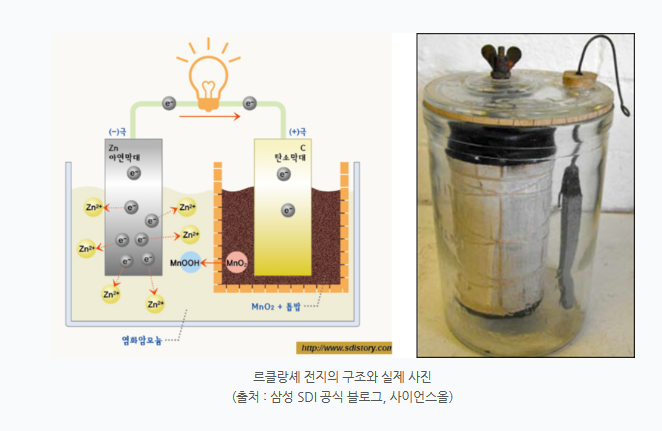 |
건전지의 구조/ 1차 전지, 2차 전지
구조는 원통 모양 또는 사각기둥 모양이며, 바깥쪽은 음극 아연제의 원통으로 용기를 겸하고 있습니다.
중앙에 탄소막대((-) 극에서 이동한 전자를 모아 공급하는 역할을 하기 때문에 집전장치라고도 불립니다.) 양극이 있으며, 그 주위에는 이산화망가니즈와 흑연을 섞어 반죽한 것을 고압에서 압착시켜서 만들었습니다.
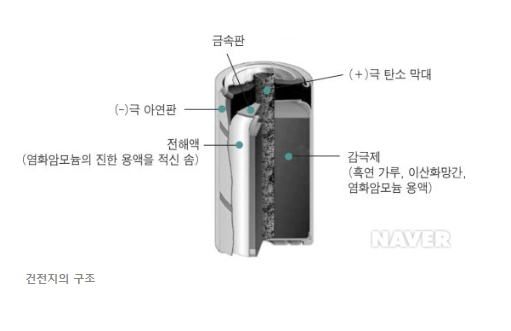
그 바깥쪽은 전해액(염화암모늄)을 충분히 흡수시킨 펄프·면지가 있으며, 풀로 격벽(隔壁)을 삼고, 이것으로 전해질의 저장고를 겸하는 것도 있습니다.
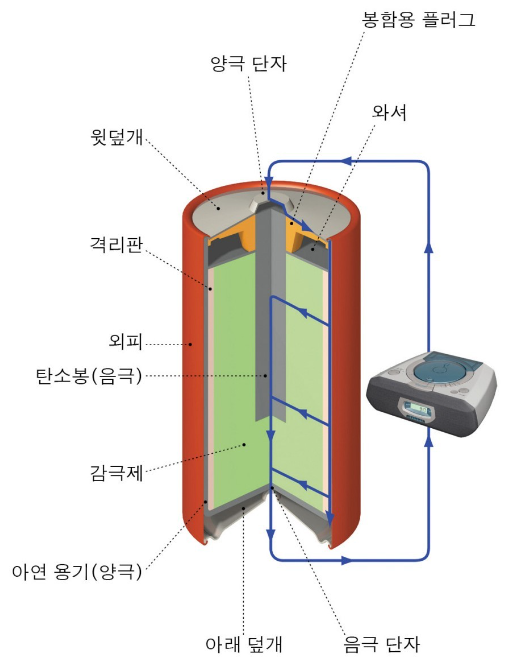
출처 : Britannica Visual Dictionary © QA International 2012.(www.ikonet.com) All rights reserved.
[1차 전지]- 한 번만 사용하도록 설계된 1회용 전지
1차 전지에는 건전지(dry cell)와 습전지(wet cell)가 있습니다. 건전지로는 아연-이산화망간 전지(알칼리), 아연-산화은 전지, 리튬-산화크롬 전지, 리튬-이산화망간 전지 등이 주로 사용되고 있다. 최근에 자동차 에너지원으로 각광을 받고 있는 연료전지도 1차전지에 속합니다.
습전지는 전해액이 수용액 상태인 전지를 말하며 볼타 전지와 다니엘 전지, 공기 전지 등이 있습니다.
그 바깥쪽은 전해액(염화암모늄)을 충분히 흡수시킨 펄프·면지가 있으며, 풀로 격벽(隔壁)을 삼고, 이것으로 전해질의 저장고를 겸하는 것도 있습니다.
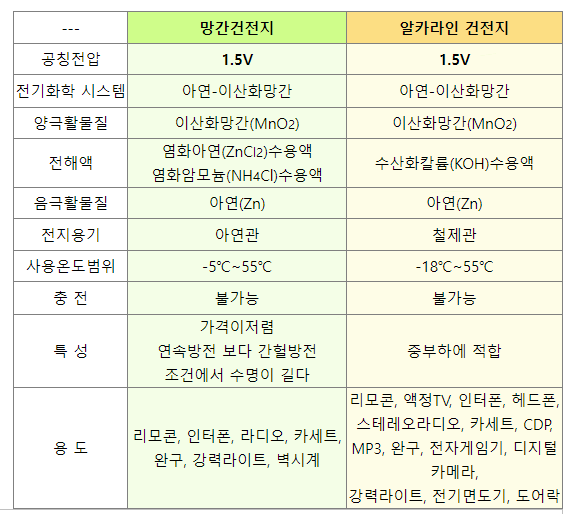
알카라인 건전지와 망간 건전지의 차이?

알카라인 건전지와 망간건전지의 가장 큰 차이는 전해질의 차이에 있습니다.
알카라인 건전지와 망간 건전지 모두 1.5v의 전압을 내고 구조 또한 아연과 이산화 망간의 결합으로 동일합니다.
전해액은 망간전지는 염화아연, 염화암모늄으로 이루어져 있습니다.
아연이 산화에 불안전해서 수병이 짧다는 단점을 보완해서 알카라인 건전지에는 강알칼리성 수용액인
수산화칼륨(KOH) 용액을 망간건전지가 자연방전율이 높은 반면 알칼라인 건전지의 자연방전률이 낮고 용량 또한 망간전지가 400~900 mAh반면 알카라인 건전지는 1,000~3,000mAh로 망간건전지보다 3배 이상 많습니다.
이러한 차이 때문에 망간건전지는 전압이 크게 필요하지 않고 저전력으로 오래 사용할 수 있는 제품에 사용합니다.
망간 전지 : 플래쉬, 리모컨, 시계, 가스 탐지기, 인터폰, 계산기
알카라인 건전지는 전력소모가 크고 모터를 돌리는 등의 강한 힘이 지속적으로 필요한 제품에 사용합니다.
알카라인 전지 : 삐삐, 면도기, 카세트, 장난감, 디지털카메라, MP3 플레이어
망간건전지는 알카라인에 비해 수명이 짧고 제품에 장기간 방치했을 때 전해액이 흘러나와 제품을 망가뜨릴 가능성이 높습니다.
알카라인 또한 장기간 방치하면 전해액이 새어 나올 수 있으므로 장기간 사용하지 않을 때는 건전지를 빼어놓도록 합니다.
망간건전지와 알카라인 건전지를 함께 사용해도 전해액이 새는 상황을 만들 수 있으므로 함께 사용하지 않습니다.


수은건전지: 미국의 s. 루벤에 의해 1947년 고안되어 P.R맬로리사에 의해서 제조된 1차 전지입니다.
루벤전지, RM전지, 수은건전지라고도 부릅니다.
아연(음전극)과, 산화수은(양극), 전해액(산화아연과 수산화칼륨)을 사용합니다.
전압은 1.35V이며 사용하는 동안 거의 일정한 전압을 유지합니다.
[2차 전지]-충전을 하여 여러 번 사용할 수 있도록 설계된 전지
화학적(chemical) 에너지를 전기적(electrical) 에너지로 변환시켜 사용이 되며 에너지가 다 방전된 상태에선
전기에너지를 공급해서 화학에너지의 형태로 다시 저장할 수 있는 전지를 말합니다.
충전과 방전을 반복할 수 있는 건전지입니다.
2차 전지는 전기에너지를 저장할 수 있기 때문에, 축전지(battery) 또는 어큐물레이터(accumulator)라고 한다.
현재 널리 사용되고 있는 2차 전지로는 납축전지, 니켈-수소(NiMH) 전지, 리튬-이온(LiO) 전지 등이 있습니다.
연축 전지 : 자동차 전지
니카드 전지 : 면도기, 무선전화기용 전지
리튬 전지 : 휴대폰, 노트북
건전지 크기에 따른 일반 명칭
망 간 : R20(DM), R14(CM), R6(AAM), R03(AAAM), 4 R25(4FM), 6 F22(FC-1)
알카라인 : LR6, LR03
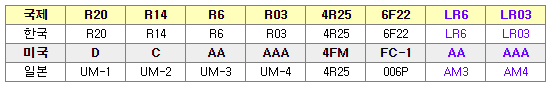

- 건전지 제조물질과 용도별 차이점
① 내부 구조 및 작용물질의 차이
>>망 간 : 이산화망간을 양극 작용물질, 아연을 음극 작용 물질, 염화암모늄
또는 염화아연 등 중성염 수용액을 전해액으로 하는 건전지
>>알카라인 : 이산화망간을 양극 작용 물질, 아연을 음극 활물질, 수산화칼륨 수용액을 전해액으로 한 전지
② 사용 용도의 차이
망간 건전지, 알카라인 건전지 모두 일반용 가전 기기에 사용되나, 소모 전류가 적으면서 오랜 시간 사용하는 탁상시계, 리모컨 등은 망간 전지가 적절하고 소모 전류가 큰 카메라, 장난감, 카세트에는 알카라인 전지가 용이합니다. - 하지만 사용 기기의 최소 사용 전압 및 소모 전류에 따라 많은 차이가 있으므로 명확히 단정 짓기는 어렵습니다.
타사 제품은 물론, 같은 회사 제품이라 할지라도, 전지의 종류나 성분에 따라 화학구성이나 방전 특성에 많은 차이를 보입니다. 따라서 전자기기에는 동일한 종류의 전지를 사용해 주세요. 때문에 전지에서 누액이 나오거나 전지가 파열될 수도 있습니다.
혼용할 경우 발생할 수 있는 현상
① 전지의 효율성 감소 :
망간건전지와 알카라인 건전지처럼 성능이 다르거나 종류가 다른 전지를 혼합하여 사용하면 알칼리전지를 사용할 수 있는 시간이 매우 짧아지며, 전압이나 형식이 다른 전지를 혼합하여 사용하면 기기가 정상적으로 동작하지 않을 뿐만 아니라 각각의 방전성능이 다르므로 빨리 소모된 전지가 과도한 사용 상태가 되어 누액의 원인이 됩니다. 또한 사용하지 않은 전지와 사용이 끝난 전지, 사용 중인 전지를 혼합하여 사용하면, 오래된 전지가 과도한 상태가 되어 비경제적일 뿐만 아니라 누액의 원인도 됩니다.
② 역충전 현상 발생 :
전압이 높은 전지는 전압이 낮은 전지를 충전하면서 소모됩니다.
-> 좀 더 정확한 말은 충전이 되는 것보다는 자가방전량을 증가시켜 용량을 소모하게 됩니다.
③ 파열 및 누액을 유발 :
전지 내부의 가스가 급격히 증가해 가스 팽창에 의한 파열 및 누액 위험발생.
혼용을 삼가야 하는 경우 ① 소모된 전지 + 새 전지 ② 충전지 + 일반 전지 ③ 알칼리 + 망간(종류가 다른 전지)
건전지를 냉장고에 보관하는 이유?
저온에서는 제품 내부의 화학반응인 이온의 활성이 약화되어 느려지는 원리를 활용한 것입니다. 저온(냉장실)에서 보관하면 실온에서 보관할 때보다 수명을 현저하게 늘릴 수는 있습니다. 냉장실 내부에 가장 찬 냉기가 품어져 나오는 곳에 건전지를 방습용 랩이나 밀폐용기에 넣어 보관하면 좋다고 합니다.
이때 건전지의 음극과 양극이 서로 닿지 않게 고무줄로 고정시켜 둬야 합니다. 하지만 건전지 보관 시 일상적인 적정 온도는 영상 10~25도에서 권장합니다. 너무 온도가 낮으면 전압이 낮아져 제대로 작동하지 않게 되고, 또 온도가 너무 높거나 습도가 높아지면 건전지의 수명이 줄어들고 급속방전이나 누액 등의 문제점이 나타나게 됩니다.
'로봇&과학 > 생활 속 과학원리' 카테고리의 다른 글
| 분리수거/재활용/새활용 (0) | 2023.04.06 |
|---|---|
| 에너지 하베스팅 (0) | 2023.02.16 |
| 도체와 부도체 실험_전기박사 (0) | 2023.02.06 |
| 플라스틱에 대하여 (0) | 2023.01.26 |
| 테스터기-과학실험 (0) | 2023.01.26 |




댓글